Чем проще опыт, тем достоверней результат
Продолжение предыдущей статьи. Обсуждение опытов.
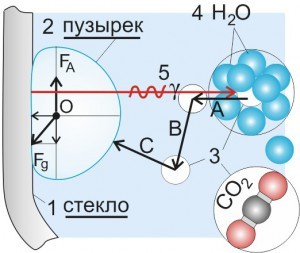
Рис. 2 (масштаб не выдержан)
1 –стенка бокала (стекло), 2 – газовый пузырек, 3 – молекула СО2, 4 - молекулы воды (12 шт.), 5 – инфракрасное излучение (крафон)
Традиционно наукой принято считать, что молекулы газа могут адсорбироваться на поверхности тремя способами: межмолекулярным взаимодействием, которое не приводит к разрыву или образованию новых химических связей; ван-дер-ваальсовыми силами; химической адсорбцией (сокращенно хемосорбцией), молекулы удерживаются на поверхности в результате образования химической, обычно ковалентной связи.
Рассмотрим ситуацию в опыте №1 (рис.2).
На поверхности стеклянного бокала 1 адсорбировался газовый пузырек 2, который образовался за счет молекул 3, растворенных в воде 4.
Во-первых, каким образом происходит «вытягивание» газовых молекул из водного чрева?
Во-вторых, что такое межмолекулярные силы?
Если молекула углекислого газа (любого газа) 3 находится в окружении 12 молекул воды 4 (для наглядности одна молекула отодвинута), то очевидно, что газовая молекула удерживается межмолекулярными силами (молекулярным притяжением) и эти силы скомпенсированы (12 апостолов – плотная упаковка). Если молекулы газа в виде пузырьков адсорбировались на стеклянной или другой твердой поверхности, то они никак не могут быть не скомпенсированы межмолекулярными силами. Молекулярные силы способны удерживать только аналогичные или меньшие по величине противостоящие силы. В объеме жидкости 12 молекул воды могут противостоять одной молекуле газа и не выпускать ее в атмосферу, препятствуя выталкивающей силе Архимеда. Когда молекулы газа вырываются из цепких лап молекул воды и устремляются либо в горизонтальном направлении, либо вертикально вниз, где объединяются между собой, образуя пузыри на поверхности стенок и на дне, то эту работу может осуществить только более мощная сила.
Молекулы газа также не «вальсируют» под управлением Ван-дер-вальса – музыки не слышно. К ван-дер-ваальсовым силам относятся взаимодействия между диполями (постоянными и индуцированными). Диполи в водной среде, в ячейке пребывания молекулы газа, могут образоваться только тогда, когда она уже покинет ячейку. Здесь также нет хемосорбции, т.к. воздух не вступает в реакцию со стеклом и другими твердыми стенками.
Гравитация и адсорбция
Только опираясь на мою гипотезу «фотонно-квантовой гравитации» можно корректно объяснить появление такого явления как адсорбция газовых пузырьков на поверхности раздела фаз жидкость-твердое, жидкость-газ. В опытах по адсорбции газовых молекул всю работу проделывают те самые неуловимые в физике – гравитоны, которые я отождествляю с электромагнитными волнами (ЭМВ). В данном случае ЭМВ инфракрасного диапазона, или красные фотоны, для краткости – крафоны!
В опыте №1 бокал имеет комнатную температуру, а водопроводная вода на 6 градусов холоднее. Крафоны 5 более нагретого тела (стекла) интенсивно обстреливают объем воды, на их пути встречаются более легкие молекулы газа, которые удерживаются в водном растворе межмолекулярными силами. Атомы молекулярного газа взаимодействуют с крафонами на полевом уровне. В результате возникает взаимное притяжение (как это происходит можно прочесть в статье: «Сила гравитации»). Газовая молекула получает механический импульс движения навстречу крафону, т.е. к стеклу (на рис. 2, вектор А). На поверхности стекла ее уже «обрабатывают» другие крафоны, коих там огромное количество, которые не позволяют ей сдвинуться с места. В это же время в данную точку подлетают другие молекулы и объединяются с первой. После воссоединения нескольких молекул появляется пузырек, который, к тому времени, становится энергонасыщенный, он сам начинает притягивать близлежащие молекулы газа, за счет которых и растет. Такие же пузырьки появляются на соседних участках, собирая вокруг себя подобные молекулы. В результате такой работы наблюдатель видит газовые пузырьки, разделенные между собой промежутками.
Следует отметить, что путь газовой молекулы до стенки стекла, не всегда пролегает по прямой линии. Дело в том, что когда молекула приобретает квант энергии и начинает двигаться навстречу прилетевшего крафона, она вскоре излучает этот квант, после чего вектор ее движения может измениться в направлении импульса придачи (на рисунке – вектор В). Об этом импульсе можно прочесть в статье: «Гравитационное излучение источника» и др. Далее молекула СО2 может опять получить новый квант энергии от другого крафона и получить очередной импульс притяжения и т.д. Таким образом, лавируя в броуновском движении, газовая молекула может влиться в какой-либо пузырек по вектору С.
На пузырек действуют две основные силы: сила Архимеда FA и сила гравитации Fg. Противостояние этих сил длится до тех пор, пока пузырек не наберет критического объема и не взлетит на поверхность. В пузырьке диаметром 0,5 мм содержится 1,752·1015 молекул!
Вот так по прямой или ломаной линии происходит движение газовой молекулы, которая в конце пути адсорбируется на поверхности раздела сред! Эта среда, как правило, имеет более высокую температуру и является адсорбентом для газового адсорбата.
Теплота порождает адсорбцию!
Теплота порождает гравитацию!
Гравитация порождает адсорбцию!
Опыты №2 и №3 с газированной водой инвертированы друг относительно друга и демонстрируют ту же закономерность, что и опыт №1. Адсорбция в бокалах наблюдается, когда температура стенок выше температуры воды.
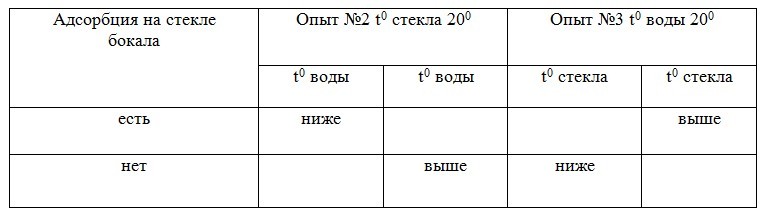
Результаты данных опытов представлены в таблице.
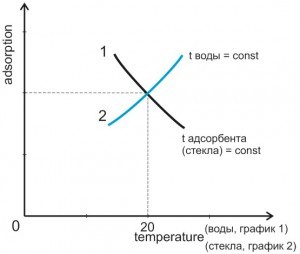
Зависимость адсорбции от температуры можно представить в виде двух графиков, направленных в разные стороны (рис.3). A=f(T)
Рис. 3
Зависимость адсорбции на стенках стекла от температуры воды
На графике №1 температура бокалов (адсорбентов) равна 200, а температура воды разная. Адсорбция, осажденного газа на стенках стеклянного бокала с повышением температуры воды, уменьшается. На графике №2 при повышении температуры бокала – адсорбция повышается.
Посмотрите видео внизу статьи.
В опыте №4 в тефлоновой сковородке несколько крупных пузырей образовались в момент наполнения водой из крана. Они возникли в момент падания первой порции воды, т.к. в этот момент была самая большая разность температур между поверхностью сковороды и водой. По мере наполнения температуры воды и сковородки постепенно выровнялись.
Перед самым моментом кипения на дне сковородки возникали пузыри пара диаметром до 8-10 мм. С такими огромными пузырями не справляется архимедова сила. Некоторые из них не взлетают вверх, а за счет конвективных потоков воды перемещаются по дну к стенке, и уже по ней поднимаются на поверхность. Скольжение по тефлоновому покрытию говорит только об одном, что крафоны от нагретой сковородки прочно удерживают паровые пузыри на ее дне. Такое скатывание пузырей ассоциируется, как будто они находятся под вакуумом.
В начале опытов я не зря измерял температуру в бокалах, т.к. все адсорбционные процессы, а я их отношу к гравитационным, связаны самым тесным образом с теплотой. Более крупные пузырьки на дне сковородки означает только одно, что дно имеет большую температуру и излучает крафоны с большей частотой и с большей энергией.
Все процессы, связанные с притяжением к Земле, предметов, пылинок, молекул и атомов друг к дугу происходят по закону гравитации, по закону Всемирного притяжения. В приведенном опыте с адсорбционными пузырьками – их появление на свет, объединение (увеличение), слипание между собой, прилипание к стенкам твердого тела, происходит не под действием каких-то загадочных ван-дер-ваальсовых сил или фантастического адсорбционного силового поля, а за счет силы гравитации!
«При повышении температуры адсорбция веществ из растворов обычно уменьшается» [6], так написано в некоторых учебниках по химии. Мои простые опыты показывают обратную картину. А именно, при повышении температуры адсорбция идет интенсивней. Притом, чем больше разница в температурах адсорбента и адсорбтива, то адсорбция идет более интенсивно. Адсорбция зависит от разности температур на разделе фаз. Если температура адсорбента выше, то адсорбция идет на поверхности адсорбента (стекле). Если температура адсорбтива выше чем температура адсорбента, то адсорбция газа идет в воде.
Еще одна популярная фраза из учебников химии: «Адсорбция протекает самопроизвольно!» [7]. Должен повторить свою мысль, что в природе ничего произвольно и вечно не делается. Все процессы, в том числе и адсорбция газа на твердом теле, идут под управлением разности потенциалов – под разностью тепловой энергии. В данном случае, элементарные опыты с обычной водопроводной и газированной водой подтверждают высказанную мысль.
Поверхностная адсорбция или просто адсорбция – всеобщее и повсеместное явление, имеющее место всегда и везде, где есть поверхность раздела между фазами и есть разность температур между этими фазами.
Адсорбционное равновесие следует всегда рассматривать при постоянной температуре.
Сила, которая вытаскивает молекулы газа, растворенные в водной среде – это сила гравитации!
Источники
- Справочник химика, http://chem21.info/info/1118166/
- Жданов Л.С., Учебник по физике, «Наука», М., 1977, (с. 93)
- Физическая энциклопедия, Академик, 2000-2014, http://dic.academic.ru/dic.nsf/enc_physics/35/
- Википедия, Политетрафторэтилен, https://ru.wikipedia.org
- Ершов Г.Д., Гравитационное излучение источника, http://gennady-ershov.ru/gravitaciya/gravitacionnoe-izluchenie-istochnika.html
- Молекулярная адсорбция из растворов на твердых адсорбентах, http://studopedia.org/1-7479.html
- Коровин Н.В., Общая химия, М., «высшая школа», 1998, Адсорбция, (с. 159), https://vk.com/doc41508733_259995962?hash=f22c58116fd38d47e1&dl=c1f8ca0c217aef2890
Опыт №2
Опыт №3
Опыт №4,№5






С выводами гораздо хуже. 1.Главная ошибка — прямая аналогия между гравитацией и электромвгнитными силами. 2.Движение навстречу импульсу возможно только у «отрицательной мвссы», которой молекулы газв, конечно, не обладают. 3.Выделоние пузырьков происходит из водных кластеров, непосредственно прилегвюших к стенкам и дну. Чтобы убедиться, откачайте часть жидкости из середины а другой бокал с помощью сифона из пластмассовой трубки. 4.Рост пузырьков за счет повышения их энергии невозможен — все самопроизвольные процессы идут в сторону понижения энергии. Кстати, самопроизвольный ознвчает незвисимый от Вашего желания. 5.Чтобы убедиться в безотносителаости адсорбции к гравитации налейте воды в поллитровую банку до краёв,закройте пластмассовой крышкой и переверните. Увидите пузырьки на дне. И т.д.
По пунктам, так по пунктам.
1. «аналогия между гравитацией и электромагнитными силами».
Я не провожу аналогию между электромагнитными силами. Я отождествляю электромагнитные волны с гравитационными волнами (гравитонами). На этом строится моя гипотеза «Фотонно-квантовой гравитации».
2. Речь не идет о заряженных частицах
3. «Выделение пузырьков происходит из водных кластеров, непосредственно прилегающих к стенкам и дну».
Соглашусь только отчасти. Адсорбция идет до тех пор, пока температуры воды и стекла не сравняются. Поэтому сначала интенсивный отсос молекул идет в пристеночных областях.
4. «Рост пузырьков за счет повышения их энергии невозможен — все самопроизвольные процессы идут в сторону понижения энергии».
Должен повторить свою мысль, что в природе ничего произвольно и вечно не делается. Все процессы, в том числе и адсорбция газа на твердом теле, идут под управлением разности потенциалов – в данном случае, под разностью тепловой энергии.
5. Оставшиеся пузырьки на дне как раз и говорят о том, что работает гравитация. Эти пузырьки выделились в момент переворота, когда дно стояло в вертикальном либо наклонном положении.